Fisiologia da dor e terminologia IASP – atualizado em 25/06/2022
A dor está associada a uma resposta de stress neuroendócrino proporcional à sua intensidade. A resposta hormonal, que é consequência da dor, resulta da ativação do sistema nervoso simpático e de reflexos mediados pelo hipotálamo. A dor, quando não controlada, tem o potencial de afetar quase todas as funções do organismo.
Fisiopatologia da dor
Em um mecanismo típico, estímulos mecânicos, químicos ou térmicos são compreendidos por terminações nervosas de neurônios primários nociceptivos, através de receptores específicos. Tal estímulo promove abertura dos canais de Na+, que geram um potencial de ação. Se o estímulo é forte o suficiente para atingir o limiar de ação, os canais voltagem dependentes se abrem, promovendo o influxo de Na+ a partir do axônio.

Nos terminais nervosos (próximo a fenda sináptica), os canais de Ca2+ se abrem e transportam as vesículas contendo neurotransmissores (principalmente glutamato) para a membrana, liberando-os na fenda sináptica.

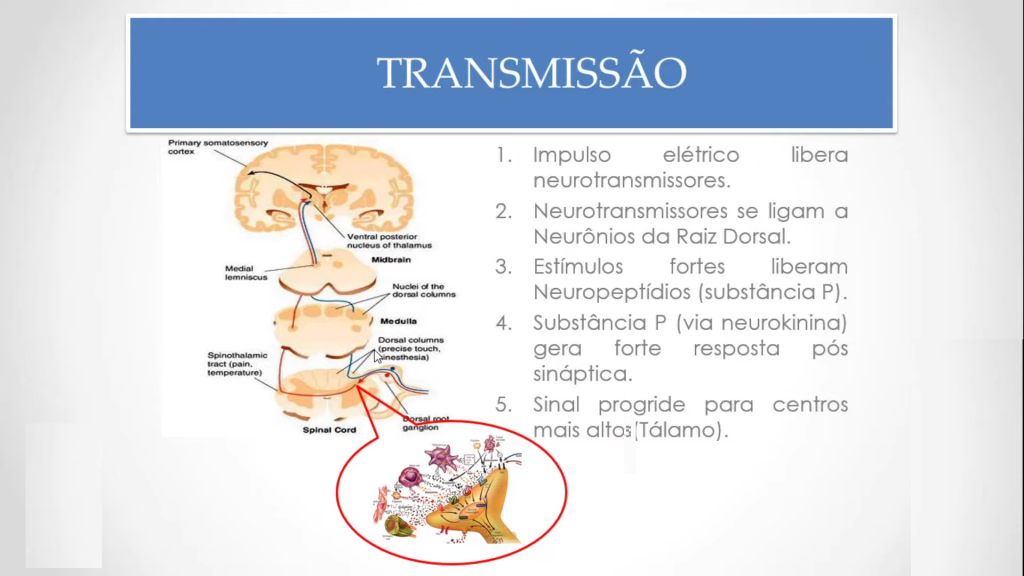
Uma vez liberados, neurotransmissores excitatórios, se ligam a receptores específicos que excitam os neurônios de projeção presentes na medula, cuja função é enviar a transmissão nervosa ao encéfalo.
Um estímulo inicial causa uma série de mudanças fisiológicas que iniciam a transmissão nervosa para a medula a partir de um neurônio sensorial nociceptivo periférico, comunicando-se enfim com o encéfalo.

Via ascendente da dor
Nos cornos dorsais, os neurônios primários formam sinapses com neurônios secundários e interneurônios localizados em várias lâminas do corno dorsal; os neurônios secundários cruzam a linha média antes de ascenderem para os núcleos supraespinhais. As fibras Aδ(delta) inervam as células da zona marginal e as fibras C inervam sobretudo as células da substância gelatinosa.
Os neurônios secundários com corpos celulares com origem nas lâminas I e II são específicas para os estímulos dolorosos de origem mecânica ou térmica e formam o trato neoespinotalâmico que transmite a informação para o córtex. Os neurônios secundários cujos corpos celulares se localizam na lâmina V são polimodais ou inespecíficos, transmitindo estímulos dolorosos de origem táctil, muscular ou visceral e também estímulos inócuos; formam o trato paleoespinotalâmico que envia a informação mais vaga para a formação reticular, a protuberância, o sistema límbico e o mesencéfalo. As qualidades afetivas aversivas da dor são percebidas depois do processamento dos sinais recebidos através do trato paleoespinotalâmico.

A dor resulta da ativação, lesão ou disfunção dos neurônios aferentes primários específicos (nociceptores) ou do sistema nervoso central (SNC). O estímulo doloroso no corpo é levado do nervo periférico até a medula espinhal, onde estas fibras fazem sinapse (contato) em um segundo neurônio localizado no corno posterior da medula. No caso do crânio, essas fibras fazem sinapse no núcleo do nervo trigêmio.
As informações ascendentes interligam-se com áreas do cérebro responsáveis pela memória e com
áreas que modulam os cornos dorsais através das vias descendentes.

A partir deste segundo neurônio, origina-se a via dolorosa conhecida como sistema espinotalâmico, o qual cruza (decussa) para o lado contralateral e ascende até o tálamo. Após o tálamo o estímulo se distribui para várias área do cérebro, chegando ao córtex; do tálamo ao córtex a dor já é consciente.

Transmissão da informação nociceptiva da medula espinal ao tálamo
O processamento central da dor, vai ocorrer em cinco vias ascendentes principais: tratos espinotalâmico, espinorreticular, espinomesencefálico, cervicotalâmico e espino-hipotalâmico.

A via do trato espinotalâmico recebe impulsos de neurônios nociceptores específicos (apenas fibras A delta e C), termossensíveis, e de amplo espectro dinâmico das lâminas I, V, VI e VII do corno dorsal. Em seguida, cruza a linha central da coluna espinal e ascendem até os núcleos talâmicos, onde o impulso elétrico provoca a sensação de dor (Lent, 2008; Kandel, 2014).
O trato espinorreticular possui os axônios dos neurônios de projeção das lâminas VII e VIII do corno dorsal sem cruzar a linha média, ascende da medula espinhal e termina na formação reticular e no tálamo.

O trato espinomesencefálico, por sua vez, projeta a partir das lâminas I e V, e possui projeção para a amígdala que contribui para o componente afetivo da dor.
O trato cervicotalâmico recebe sinal das lâminas III e IV do corno dorsal e ascende no tronco encefálico até chegar ao tálamo.
O trato espino-hipotalâmico, por sua vez, abriga os axônios dos neurônios presentes nas lâminas I, V e VIII do corno da medula, e regulam respostas neuroendócrinas e cardiovasculares nas síndromes dolorosas (Lent, 2008; Kandel, 2014).

O tálamo desempenha um papel muito importante na integração do impulso doloroso. A partir dele, neurônios de terceira ordem transmitem impulsos para o córtex cerebral, onde ocorre o processamento que resulta em consciência da dor.
Via Descendente ou de Supressão da Dor
Existem três mecanismos de supressão da dor: a inibição segmentar, o sistema opioide endógeno e o sistema inibitório descendente.
A teoria da inibição segmentar (teoria do portão) propõe que a transmissão dos estímulos através das sinapses entre as fibras Aδ e C e as células dos cornos dorsais da medula pode ser atenuada ou bloqueada. As fibras Aα e Aβ que transmitem estímulos inócuos, como o toque, estimulam interneurônios que inibem a transmissão sináptica. Este mecanismo explicaria porque o esfregar a área lesada reduz a dor. Também a ação da estimulação elétrica transcutânea dos nervos, conhecida pela sigla TENS, poderia ser explicada por este mecanismo.
Os opioides endógenos (encefalinas, endorfinas e dinorfina) podem inibir a dor ligando-se aos receptores opioides a nível da medula. São péptidos segregados do SNC em momentos de dor intensa, de stress ou de ambos.
O sistema inibitório descendente é outro dos mecanismos de modulação da dor. Uma das vias deste sistema tem origem na substância cinzenta periaqueductal no mesencéfalo, com sinapses no núcleo magno da rafe, de onde se projetam fibras para a medula espinal, cujo neurotransmissor é a serotonina. A outra tem origem no núcleo ceruleus na protuberância que tem projeções para a medula espinal, cujo neurotransmissor é a noradrenalina. A ativação do sistema descendente da dor inibe a transmissão dos estímulos dolorosos nas sinapses no corno dorsal da medula pela ação dos opioides endógenos.
É o principal mecanismo que o sistema nervoso utiliza para reduzir a dor. Descendo do córtex cerebral, o sistema descendente vai recebendo várias vias (aferências), dentre as quais as mais conhecidas são a substância cinzenta periaquedutal e a medula rostroventromedial. Para reduzir a dor os principais transmissores do sistema descendente, são a serotonina e noradrenalina, os quais em seguida induzem a liberação de opioides endógenos (substâncias estas similares a morfina) no corno posterior da medula, levando ao efeito analgésico. Este mecanismo explica em parte a inter-relação entre dor e depressão uma vez que utilizam alguns transmissores em comum.
Aumentar atividade analgésica do sistema descendente é um dos pilares na terapia da dor, uma vez que várias síndromes dolorosas cursam com hipoatividade no sistema descendente. Na fibromialgia por exemplo, acredita-se que o sistema descendente esteja hipoativo, levando a um aumento na percepção da sensação dolorosa.
Atualmente sabe-se que o sistema descendente pode ser ativado de múltiplas formas incluindo mecanismo farmacológico como os antidepressivos amitriptilina e duloxetina, e, mecanismos não farmacológicos como acupuntura, estimulação elétrica transcutânea, estimulação magnética transcraniana, etc. Um conjunto de atividades comportamentais também podem ser utilizados para aumentar a atividade do sistema descendente como exercício físico regular, uma boa noite de sono, exercícios de relaxamento e qualquer mudança que melhore a qualidade de vida.
Há uma série de eventos e mediadores químicos que tornam muito complexo esse processo. Embora relevante, o estudo específico da fisiologia da dor ultrapassa o objetivo dessa postagem, que é o estudo da dor para seu correto manejo clínico. Quem desejar se aprofundar na fisiopatologia da dor, sugiro a leitura dessa página abaixo.
Reflexo de retirada e reflexo extensor cruzado
A medula espinhal não é apenas um caminho para conexões motoras e sensoriais entre o sistema nervoso periférico e o encéfalo, é também responsável pela coordenação de reflexos sensoriais-motores. Os sinais sensoriais entram na medula (exclusivamente via raízes dorsais) onde fazem sinapses com neurônios motores anteriores ou com interneurônios. Os neurônios motores anteriores deixam a medula via raízes ventrais e inervam diretamente as fibras musculares esqueléticas.
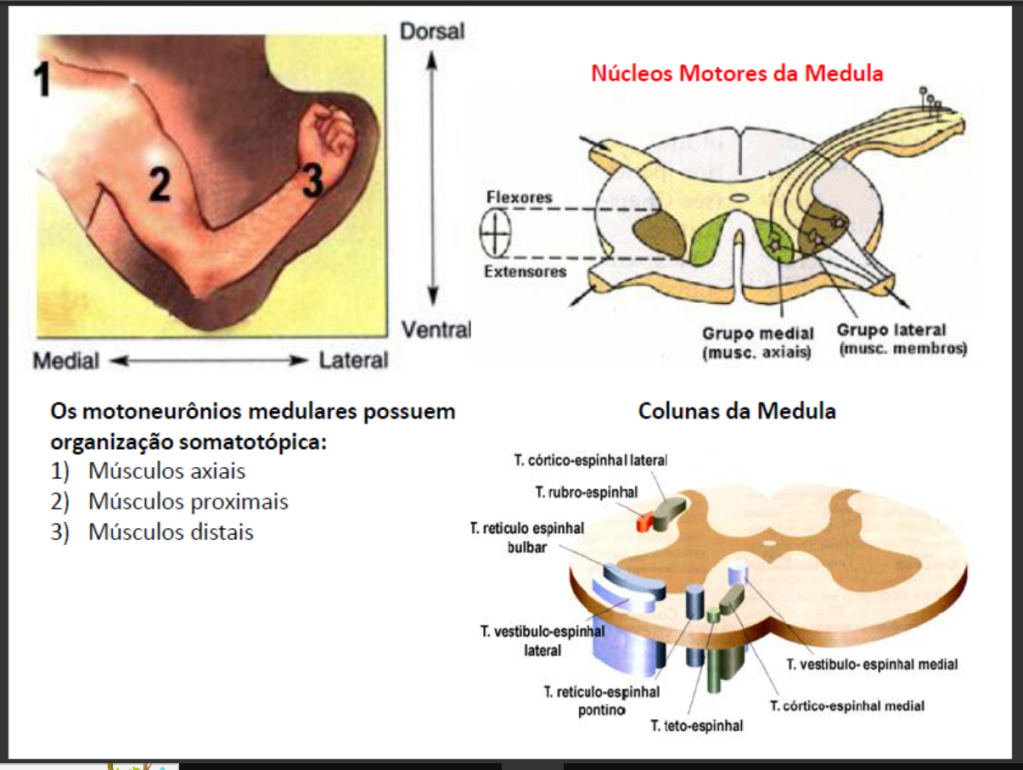
Os interneurônios ficam confinados ao sistema nervoso central e fazem conexões tanto com neurônios sensoriais quanto com neurônios motores.

Na maioria das vezes os sinais sensoriais são transmitidos primeiramente para os interneurônios, onde são adequadamente processados, antes de convergirem sobre os neurônios motores anteriores para o controle da função muscular. Portanto, os sinais sensoriais que chegam à medula podem provocar uma resposta motora direta, ao fazerem sinapse com neurônios motores anteriores (reflexo monossináptico) ou indireta, ao fazerem sinapse com os interneurônios.
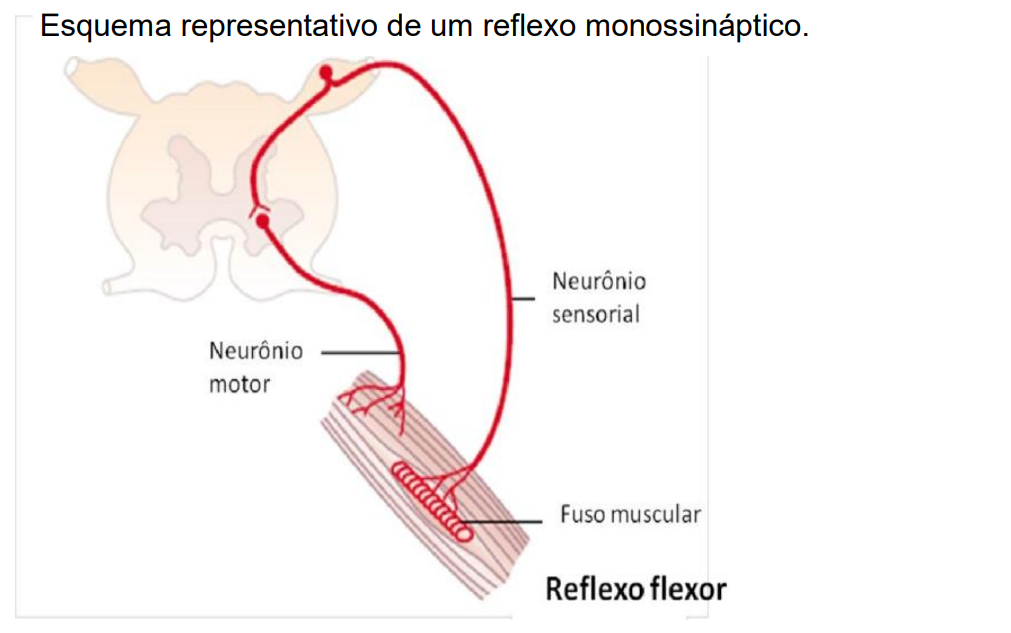
Dentre os reflexos medulares está o reflexo flexor ou de retirada. Este reflexo é caracterizado pela retirada de um membro do corpo frente a estímulos como dor, picada e calor. Um exemplo é quando encostamos a mão no fogo: não precisamos ver ou mesmo sentir a dor para que a resposta reflexa seja desencadeada e nossa mão seja retirada (reflexo flexor ou de retirada). Isso ocorre graças à integração, na medula, da ativação dos neurônios sensitivos com os neurônios motores e, consequente excitação dos músculos flexores e recíproco relaxamento ou inibição dos músculos extensores.
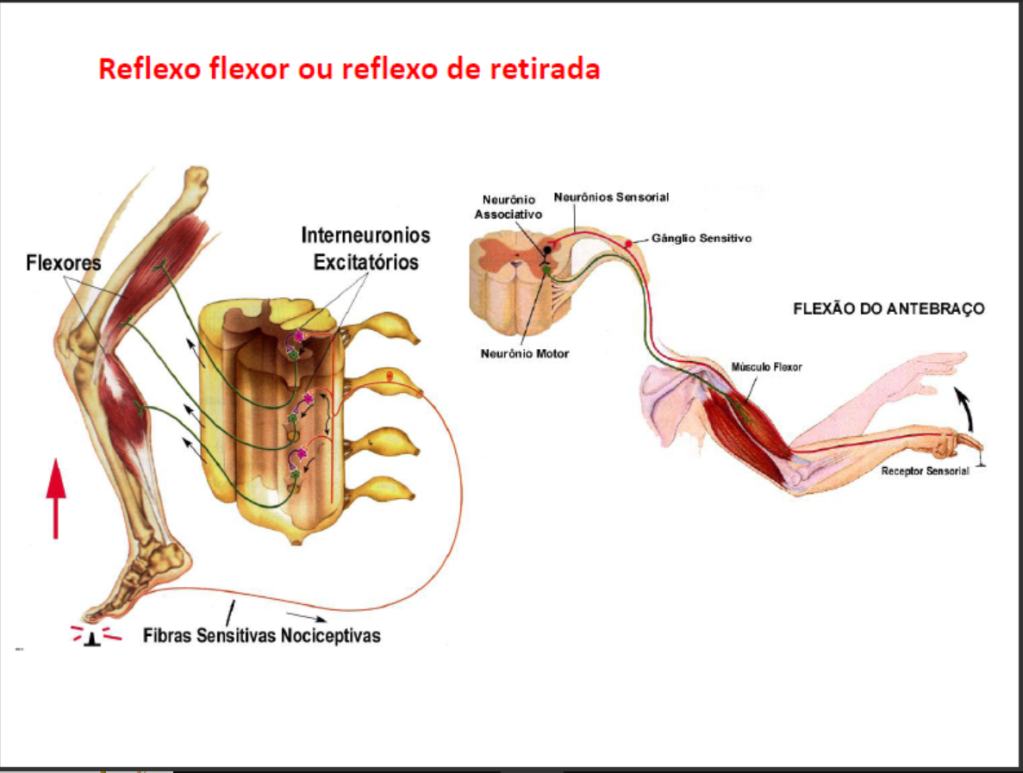
A flexão de um membro acompanhada da reação contralateral do membro oposto é denominada reflexo extensor cruzado. No entanto, para que este reflexo seja observado o estímulo tem que ser suficientemente forte para atingir os interneurônios, com limiar de ativação mais alto, que fazem parte do circuito neuronal do reflexo extensor cruzado. A necessidade do envolvimento dos músculos contralaterais neste tipo de reflexo tem a função de dar suporte postural durante a retirada do membro afetado frente ao estímulo da dor.
Terminologia atualizada da Associação Internacional de Estudo da Dor (IASP)

O trabalho da Força-Tarefa em Taxonomia da época de 1979 a 1994 foi continuado pelo Comitê de Taxonomia que atualizou o termo “dor” e a classificação das síndromes de dor. Todos os termos foram cuidadosamente revisados e sua utilidade avaliada em relação aos novos conhecimentos sobre os aspectos clínicos e científicos básicos da dor. Conforme declarado em publicações anteriores da taxonomia IASP, não vemos esta lista de termos como imutável. À medida que aprendemos mais sobre a dor, precisaremos atualizar a terminologia.
DOR
Uma experiência sensorial e emocional desagradável associada ou semelhante a uma lesão tecidual real ou potencial.
Seis pontos-chave e etimologia:
1) A dor é sempre uma experiência pessoal que é influenciada em graus variados por fatores biológicos, psicológicos e sociais.
2) Dor e nocicepção são fenômenos diferentes. A dor não pode ser inferida apenas pela atividade nos neurônios sensoriais.
3) Através de suas experiências de vida, os indivíduos aprendem o conceito de dor.
4) O relato de uma pessoa de uma experiência como dor deve ser respeitado.
5) Embora a dor geralmente tenha um papel adaptativo, ela pode ter efeitos adversos na função e no bem-estar social e psicológico.
6) A descrição verbal é apenas um dos vários comportamentos para expressar dor; a incapacidade de se comunicar não nega a possibilidade de um animal humano ou não humano sentir dor.
Etimologia: Inglês médio, do anglo-francês peine (dor, sofrimento), do latim poena (penalidade, punição), por sua vez do grego poine (pagamento, penalidade, recompensa).
Uma mudança central na nova definição, em comparação com a versão de 1979, está substituindo a terminologia que dependia da capacidade de uma pessoa de descrever a experiência para se qualificar como dor. A antiga definição dizia: “Uma experiência sensorial e emocional desagradável associada a dano tecidual real ou potencial, ou descrita em termos de tal dano”. Essa redação foi interpretada como excluindo bebês, idosos e outros – até mesmo animais – que não conseguiam articular verbalmente sua dor, disse o Dr. Jeffrey Mogil, diretor do Alan Edwards Center for Research on Pain, McGill University e membro da força-tarefa.
ALODINIA
Dor devido a um estímulo que normalmente não provocaria dor.
Nota: O estímulo leva a uma resposta inesperadamente dolorosa. Este é um termo clínico que não implica um mecanismo. A alodinia pode ser observada após diferentes tipos de estímulos somatossensoriais aplicados a muitos tecidos diferentes.
O termo alodínia foi originalmente introduzido para separar hiperalgesia e hiperestesia, as condições observadas em pacientes com lesões do sistema nervoso em que toque, pressão leve ou frio ou calor moderados evocam dor quando aplicados em pele aparentemente normal. “Allo” significa "outro" em grego e é um prefixo comum para condições médicas que divergem do esperado. “Odynia” é derivado da palavra grega "odune" ou "odyne", que é usada em "pleurodinia" e "coccidínia" e é semelhante em significado à raiz da qual derivamos palavras com -algia ou -algesia nelas. Alodinia foi sugerida após discussões com o professor Paul Potter, do Departamento de História da Medicina e Ciência da Universidade de Western Ontario.
ANESTESIA DOLOROSA
Dor em uma área ou região que esta anestesiada anestésica.
CAUSALGIA
Síndrome de dor em queimação sustentada, alodinia e hiperpatia após uma lesão nervosa traumática, muitas vezes combinada com disfunção vasomotora e sudomotora e alterações tróficas posteriores.
DISESTESIA
Uma sensação anormal desagradável, espontânea ou evocada.
Nota: Comparar com dor e parestesia. Casos especiais de disestesia incluem hiperalgesia e alodinia. Uma disestesia deve ser sempre desagradável e uma parestesia não deve ser desagradável, embora se reconheça que o limítrofe pode apresentar algumas dificuldades na hora de decidir se uma sensação é agradável ou desagradável. Deve-se sempre especificar se as sensações são espontâneas ou evocadas.
HIPERALGESIA
Aumento da dor a partir de um estímulo que normalmente provoca dor.
Nota: A hiperalgesia reflete o aumento da dor na estimulação supralimiar(acima do limite a partir do qual ocorre dor). Este é um termo clínico que não implica um mecanismo. Para a dor evocada por estímulos que geralmente não são dolorosos, o termo alodinia é preferido, enquanto a hiperalgesia é mais apropriada para casos com resposta aumentada em um limiar normal ou em um limiar aumentado, por exemplo, em pacientes com neuropatia. Também deve ser reconhecido que na alodinia o estímulo e a resposta estão em modos diferentes, enquanto na hiperalgesia eles estão no mesmo modo. As evidências atuais sugerem que a hiperalgesia é uma consequência da perturbação do sistema nociceptivo com sensibilização periférica ou central, ou ambas, mas é importante distinguir entre os fenômenos clínicos, que essa definição enfatiza, e a interpretação, que pode mudar à medida que o conhecimento avança . A hiperalgesia pode ser observada após diferentes tipos de estimulação somatossensorial aplicada a diferentes tecidos.
HIPERESTESIA
Aumento da sensibilidade à estimulação, excluindo os sentidos especiais.
Nota: O estímulo e o local devem ser especificados. A hiperestesia pode se referir a vários modos de sensibilidade cutânea, incluindo toque e sensação térmica sem dor, bem como à dor. A palavra é usada para indicar tanto um limiar diminuído a qualquer estímulo quanto uma resposta aumentada a estímulos que são normalmente reconhecidos.
Alodinia é sugerida para dor após estimulação que normalmente não é dolorosa. A hiperestesia inclui tanto alodinia quanto hiperalgesia, mas os termos mais específicos devem ser usados onde quer que sejam aplicáveis.
HIPERPATIA
Síndrome dolorosa caracterizada por uma reação anormalmente dolorosa a um estímulo, especialmente um estímulo repetitivo, bem como um limiar aumentado.
Nota: Pode ocorrer com alodinia, hiperestesia, hiperalgesia ou disestesia. Falha na identificação e localização do estímulo, atraso, sensação de irradiação e sensação posterior podem estar presentes, e a dor é frequentemente de caráter explosivo.
HIPOALGESIA
Dor diminuída em resposta a um estímulo normalmente doloroso.
Nota: A hipoalgesia era anteriormente definida como sensibilidade diminuída à estimulação nociva, tornando-se um caso particular de hipoestesia. No entanto, agora se refere apenas à ocorrência de relativamente menos dor em resposta à estimulação que produziria dor. A hipoestesia abrange o caso de diminuição da sensibilidade à estimulação que normalmente é dolorosa.
HIPOESTESIA
Diminuição da sensibilidade à estimulação, excluindo os sentidos especiais.
Nota: Estimulação e localização para ser especificada.
TRATAMENTO INTERDISCIPLINAR
Tratamento multimodal fornecido por uma equipe multidisciplinar, colaborando na avaliação e tratamento usando um modelo e objetivos biopsicossociais compartilhados. Por exemplo: a prescrição de um antidepressivo por um médico juntamente com o tratamento de exercícios por um fisioterapeuta e o tratamento cognitivo-comportamental por um psicólogo, todos trabalhando em conjunto com reuniões regulares de equipe (presencial ou online), acordo sobre diagnóstico, objetivos terapêuticos e planos para tratamento e revisão.
TRATAMENTO MULTIDISCIPLINAR
Tratamento multimodal fornecido por profissionais de diferentes disciplinas. Por exemplo: a prescrição de um antidepressivo por um médico juntamente com o tratamento de exercícios por um fisioterapeuta e o tratamento cognitivo-comportamental por um psicólogo, todas as profissões trabalhando separadamente com seu próprio objetivo terapêutico para o paciente e não necessariamente se comunicando.
TRATAMENTO MULTIMODAL
O uso simultâneo de intervenções terapêuticas separadas com diferentes mecanismos de ação dentro de uma disciplina visava diferentes mecanismos de dor. Por exemplo: o uso de pregabalina e opioides para controle da dor por um médico; o uso de AINE e órtese para controle da dor por um médico.
NEURALGIA
Dor na distribuição de um nervo ou nervos.
Nota: O uso comum, especialmente na Europa, muitas vezes implica uma qualidade paroxística, mas a neuralgia não deve ser reservada para dores paroxísticas.
NEURITE
Inflamação de um nervo ou nervos.
Nota: Não deve ser usado a menos que a inflamação esteja presente.
DOR NEUROPÁTICA
Dor causada por uma lesão ou doença do sistema nervoso somatossensorial.
Nota: A dor neuropática é uma descrição clínica (e não um diagnóstico) que requer uma lesão demonstrável ou uma doença que satisfaça os critérios diagnósticos neurológicos estabelecidos. O termo lesão é comumente usado quando investigações diagnósticas (por exemplo, imagem, neurofisiologia, biópsias, exames laboratoriais) revelam uma anormalidade ou quando houve trauma óbvio. O termo doença é comumente usado quando a causa subjacente da lesão é conhecida (por exemplo, acidente vascular cerebral, vasculite, diabetes mellitus, anormalidade genética).
Somatossensorial refere-se a informações sobre o corpo em si, incluindo órgãos viscerais, em vez de informações sobre o mundo externo (por exemplo, visão, audição ou olfato). A presença de sintomas ou sinais (por exemplo, dor evocada pelo toque) por si só não justifica o uso do termo neuropático. Algumas entidades de doença, como a neuralgia do trigêmeo, são atualmente definidas por sua apresentação clínica e não por testes diagnósticos objetivos. Outros diagnósticos, como neuralgia pós-herpética, normalmente são baseados na história. É comum ao investigar a dor neuropática que os testes diagnósticos possam produzir dados inconclusivos ou mesmo inconsistentes. Nesses casos, o julgamento clínico é necessário para reduzir a totalidade dos achados de um paciente em um diagnóstico ou grupo conciso de diagnósticos.
DOR NEUROPÁTICA CENTRAL
Dor causada por uma lesão ou doença do sistema nervoso somatossensorial central. Veja nota de dor neuropática.
DOR NEUROPÁTICA PERIFÉRICA
Dor causada por uma lesão ou doença do sistema nervoso somatossensorial periférico. Veja nota de dor neuropática.
NEUROPATIA
Um distúrbio da função ou alteração patológica do nervo. 1) Ocorrendo em um nervo, mononeuropatia; 2) ocorrendo em vários nervos, mononeuropatia múltipla; 3) ocorrendo de forma difusa e bilateral, polineuropatia.
Nota: A neurite é um caso especial de neuropatia e agora está reservada para processos inflamatórios que afetam os nervos.
NOCICEPÇÃO
O processo neural de codificação de estímulos nocivos.
Nota: As consequências da codificação podem ser autonômicas (por exemplo, pressão arterial elevada) ou comportamentais (reflexo de retirada motora ou comportamento nocifensivo mais complexo). A sensação de dor não está necessariamente implícita.
NEURÔNIO NOCICEPTIVO
Um neurônio central ou periférico do sistema nervoso somatossensorial que é capaz de codificar estímulos nocivos.
DOR NOCICEPTIVA
Dor que surge de dano real ou ameaçado ao tecido não neural e é devido à ativação de nociceptores.
Nota: Este termo é projetado para contrastar com a dor neuropática. O termo é usado para descrever a dor que ocorre com um sistema nervoso somatossensorial funcionando normalmente para contrastar com a função anormal observada na dor neuropática.
ESTÍMULO NOCICEPTIVO
Um evento de dano real ou potencial ao tecido transduzido e codificado por nociceptores.
NOCICEPTOR
Receptor sensorial de alto limiar do sistema nervoso somatossensorial periférico que é capaz de transduzir e codificar estímulos nocivos.
DOR NOCIPLÁSTICA
Dor que surge da nocicepção alterada, apesar de não haver evidência clara de dano tecidual real ou ameaçado, causando a ativação de nociceptores periféricos ou evidência de doença ou lesão do sistema somatossensorial que causa a dor.
Nota: Os pacientes podem ter uma combinação de dor nociceptiva e nociplástica
ESTÍMULO NOCIVO
Um estímulo que danifica ou ameaça danificar os tecidos normais.
O LIMIAR DE DOR
A intensidade mínima de um estímulo que é percebido como doloroso.
Nota: Tradicionalmente, o limiar tem sido frequentemente definido, como o definimos anteriormente, como a menor intensidade de estímulo na qual um sujeito percebe a dor. Devidamente definido, o limiar é realmente a experiência do paciente, enquanto a intensidade medida é um evento externo. Tem sido de uso comum para a maioria dos pesquisadores da dor definir o limiar em termos do estímulo, e isso deve ser evitado. No entanto, o estímulo limiar pode ser reconhecido como tal e medido. Na psicofísica, os limiares são definidos como o nível em que 50% dos estímulos são reconhecidos. Nesse caso, o limiar de dor seria o nível em que 50% dos estímulos seriam reconhecidos como dolorosos. O estímulo não é dor (q.v.) e não pode ser uma medida de dor.
NÍVEL DE TOLERÂNCIA À DOR
A intensidade máxima de um estímulo produtor de dor que um sujeito está disposto a aceitar em uma determinada situação.
Nota: Tal como acontece com o limiar de dor, o nível de tolerância à dor é a experiência subjetiva do indivíduo. Os estímulos que normalmente são medidos em relação à sua produção são os estímulos do nível de tolerância à dor e não o nível em si. Assim, o mesmo argumento se aplica ao nível de tolerância à dor quanto ao limiar de dor, e não é definido em termos de estimulação externa como tal.
PARESTESIA
Uma sensação anormal, espontânea ou evocada.
Nota: Comparar com disestesia. Após muita discussão, concordou-se em recomendar que a parestesia seja usada para descrever uma sensação anormal que não seja desagradável, enquanto a disestesia seja usada preferencialmente para uma sensação anormal considerada desagradável.
O uso de um termo (parestesia) para indicar sensações espontâneas e o outro para se referir a sensações evocadas não é indicado. Há um sentido em que, como a parestesia se refere a sensações anormais em geral, pode incluir disestesia, mas o inverso não é verdadeiro. A disestesia não inclui todas as sensações anormais, mas apenas aquelas que são desagradáveis.
SENSIBILIZAÇÃO
Aumento da capacidade de resposta dos neurônios nociceptivos à sua entrada normal e/ou recrutamento de uma resposta a entradas normalmente abaixo do limiar de ativação.
Nota: A sensibilização pode incluir uma queda no limiar e um aumento na resposta supralimiar. Descargas espontâneas e aumentos no tamanho do campo receptivo também podem ocorrer. Este é um termo neurofisiológico que só pode ser aplicado quando tanto a entrada quanto a saída do sistema neural em estudo são conhecidas, por exemplo, controlando o estímulo e medindo o evento neural. Clinicamente, a sensibilização só pode ser inferida indiretamente a partir de fenômenos como hiperalgesia ou alodinia.
SENSIBILIZAÇÃO CENTRAL
Aumento da responsividade dos neurônios nociceptivos no sistema nervoso central à sua entrada aferente normal ou subliminar.
Nota: Veja a nota para sensibilização e neurônio nociceptivo acima. Isso pode incluir aumento da capacidade de resposta devido à disfunção dos sistemas endógenos de controle da dor. Os neurônios periféricos estão funcionando normalmente; as mudanças na função ocorrem apenas nos neurônios centrais.
SENSIBILIZAÇÃO PERIFÉRICA
Aumento da capacidade de resposta e redução do limiar de neurônios nociceptivos na periferia à estimulação de seus campos receptivos.
Nota: Veja a nota para sensibilização acima.
TRATAMENTO UNIMODAL
Intervenção terapêutica única direcionada a um mecanismo específico de dor ou diagnóstico de dor. Por exemplo: a aplicação de tratamento de exercícios por um fisioterapeuta.
